Osteoporosis
Osteoporosis
- Epidemiología
- Remodelación ósea
- Clasificación de la osteoporosis
- Causas secundarias de pérdida ósea en el adulto
- Medidas por absorciometría de energía dual con rayos X de la densidad mineral ósea
- Otros instrumentos para medi r la masa ósea
- Evaluación del riesgo con FRAX
- Marcadores biológicos: marcadores bioquímicos del recambio óseo
- Osteoporosis inducida por glucocorticoides
- Definición
- Biología
- Pico de masa ósea
- Pérdida ósea en personas ancianas
- Mecanismos moleculares y celulares en la remodelación normal
- Mecanismos celulares y moleculares de la pérdida ósea
- Densitometría ósea
- Evaluación diagnóstica
- Osteoporosis en varones
- Lecturas Recomendadas
Epidemiología
A la edad de 50 años, el riesgo de fractura debido a la osteoporosis en una mujer blanca es de alrededor del 40%, similar al de la enfermedad cardíaca coronaria; en varones, la cifra correspondiente es del 13%. En Estados Unidos, se producen aproximadamente 350.000 fracturas de cadera, cerca de un millón de fracturas vertebrales y 200.000 fracturas de muñeca cada año. Además, otras fracturas relacionadas con la fragilidad, sobre todo las de la pelvis y el húmero, son una causa de morbilidad importante en personas ancianas. La incidencia de fracturas osteoporóticas aumenta de forma muy importante con la edad. En mujeres, este incremento se observa después de los 45 años y sobre todo se debe a fracturas del antebrazo. Después de la edad de 65 años, la incidencia de fracturas de cadera aumenta exponencialmente. En varones, la incidencia de fracturas relacionadas con la fragilidad aumenta después de los 75 años, y en ambos sexos la cadera es la localización más frecuente de fracturas después de los 85 años. La incidencia de fracturas vertebrales está peor documentada, debido a que muchos pacientes están asintomáticos. En las fracturas con repercusión clínica, se produce un incremento exponencial con la edad en varones, mientras que se produce un incremento más lineal relacionado con la edad en mujeres. El aumento de la prevalencia de fracturas con la edad es independiente del cambio de la DMO; la edad es, por sí misma, un factor de riesgo independiente para las fracturas.
Se han notificado diferencias geográficas importantes en la incidencia de fracturas osteoporóticas. Esta característica puede deberse principalmente a diferencias raciales en el tamaño del esqueleto; la osteoporosis es más frecuente en las poblaciones asiáticas y blanca, y menos frecuente en los negros africanos y americanos. En muchas partes del mundo, la evidencia indica que las fracturas osteoporóticas han aumentado de forma considerable incluso sin tener en cuenta el factor de la edad de la población. Sin embargo, un reciente estudio en individuos canadienses muestra que en los últimos 10 años se ha producido una disminución en la incidencia de fracturas de cadera. No obstante, la mayor esperanza de vida duplicará el número de fracturas de cadera en los próximos 50 años.
Las diferencias étnicas y de género desempeñan un papel principal en la epidemiología de las fracturas. Los hombres tienen una mayor densidad ósea que las mujeres y los afroamericanos tienen una DMO significativamente mayor durante su etapa adulta que los blancos, tanto en el compartimento cortical como en el trabecular. Estas diferencias se relacionan en parte con los efectos de la composición corporal, incluida la fuerza muscular, la distribución de la grasa corporal y el tamaño de los huesos. Por tanto, se producen muchas menos fracturas en los afroamericanos que en los asiáticos o los blancos, sobre todo en los blancos descendientes de europeos. Sin embargo, recientemente se está reevaluando el papel de la masa grasa en relación con la DMO. Claramente, un bajo índice de masa corporal (<20) se asocia con una baja DMO y con un mayor riesgo de fracturas. Esto, en parte, se debe a una menor conversión periférica de testosterona en estrógenos y a un menor aislamiento en los impactos. Por otra parte, las relaciones entre la masa ósea y un aumento de la masa grasa (IMC > 30) están menos claras. El aumento de la grasa subcutánea afecta de forma positiva al área ósea cortical, aunque varios estudios recientes sugieren que la grasa visceral puede tener un impacto negativo sobre la masa ósea y que se puede asociar a un mayor riesgo de fracturas. Aunque a menudo se consideraba como protectora, actualmente se conoce que la obesidad no evita las fracturas y en algunas circunstancias puede aumentar el riesgo.
Remodelación ósea
A pesar de que los traumatismos son la causa principal de fractura, los factores que alteran la calidad o la cantidad de hueso predisponen a un sujeto a fracturas osteoporóticas. Por tanto, es esencial la comprensión de la remodelación ósea para determinar cómo la masa ósea puede alterarse por influencias hereditarias y ambientales. La remodelación ósea mantiene el calcio sérico y la resistencia del hueso una vez que se ha detenido el crecimiento longitudinal. Este proceso cíclico se produce en elementos microscópicos denominados unidades multicelulares básicas o de remodelación. La remodelación ósea comienza con la disolución o resorción ósea y termina con la formación de hueso nuevo, sin producir un cambio neto de la masa ósea. En la edad adulta, cada unidad de remodelación está equilibrada, la resorción iguala a la formación, y dura entre 90 y 130 días. El mantenimiento de la masa ósea durante la remodelación asegura una fuente disponible de calcio para el cuerpo para las funciones corporales y mantiene la resistencia ósea durante los cambios en la arquitectura. Sin embargo, las unidades de remodelación pueden desequilibrarse y, tras varios ciclos, esta situación puede provocar una pérdida importante de hueso. Estos desequilibrios son el resultado de una resorción ósea mayor a la formación, y pueden ser debidos a cambios en las hormonas sistémicas, la ingesta dietética o la carga mecánica.
Clasificación de la osteoporosis
Los primeros trabajos proponían dos tipos de osteoporosis, basándose en la edad de comienzo: osteoporosis de tipo I o posmenopáusica, provocada por una privación de estrógenos en torno a la menopausia; y osteoporosis de tipo II, relacionada con un elevado recambio por déficit de calcio y de vitamina D. Sin embargo, hoy en día es evidente que este tipo de clasificación está anticuada y tiene muy poco interés clínico. Muchas mujeres jóvenes posmenopáusicas pueden tener una deficiencia de vitamina D, y los sujetos ancianos pueden sufrir tanta pérdida de hueso como las mujeres jóvenes debido a una insuficiencia progresiva de estrógenos. De forma similar, aunque las fracturas de muñeca, así como las fracturas vertebrales, son más frecuentes en las mujeres sanas posmenopáusicas más jóvenes, este tipo de fracturas es muy característico de cualquier tipo de osteoporosis y representa una alteración ósea en relación con una alteración de la cantidad o calidad del hueso, independientemente de la edad.
- Últimos artículos sobre Clasificación de la osteoporosis
- Resultados sobre osteoporosis & Clasificación de la osteoporosis
Causas secundarias de pérdida ósea en el adulto
Aunque la mayoría de las causas de osteoporosis son etiquetadas como idiopáticas y se deben a procesos celulares y moleculares relacionados con la privación de estrógenos y/o el envejecimiento, es importante excluir causas secundarias, principalmente porque estos trastornos son a veces reversibles con la resolución de la causa subyacente ( tabla 251-2 ). El hipogonadismo de cualquier causa, tanto en varones como en mujeres, es probablemente la causa más frecuente de osteoporosis secundaria, sobre todo en pacientes jóvenes. La anorexia nerviosa, la amenorrea hipotalámica, la hiperprolactinemia y la amenorrea inducida por ejercicio producen una pérdida rápida y precoz de hueso que puede conllevar fracturas osteoporóticas subsiguientes en estas situaciones y se mantienen durante un largo período de tiempo. En pacientes varones, el hipogonadismo primario o secundario produce un pico bajo de masa ósea y una pérdida significativa de hueso durante la etapa media de la vida. Los trastornos hormonales que interfieren con el eje hipotalámico gonadal normal, como la hipercortisolemia, también conllevan una masa ósea reducida. El exceso de cortisol altera la transducción de señales de la hormona liberadora de gonadotropinas, lo que provoca una disminución de las concentraciones de estrógenos o andrógenos y potencia la resorción ósea; estos cambios se acompañan de alteraciones en el reclutamiento y la función de los osteoblastos, un aumento en la adiposidad de la médula, la reducción de la transducción de señales IGF-I y la alteración en la resorción de calcio. Como resultado, la unidad de remodelación se desacopla, se produce una rápida pérdida ósea y las fracturas son un componente frecuente en este síndrome. Otros trastornos endocrinológicos se asocian con pérdida de masa ósea o con un recambio óseo elevado (v. tabla 251-2 ). Estos trastornos incluyen el hipertiroidismo grave, el hiperparatiroidismo primario y la deficiencia de hormona de crecimiento. En el hiperparatiroidismo primario, la pérdida ósea se produce principalmente en localizaciones de hueso cortical y es reversible con la extirpación quirúrgica del tumor.
Tabla 251-2
Causas secundarias de osteoporosis
| ENFERMEDADES ENDOCRINAS |
Hipogonadismo femenino
Hipogonadismo masculino
Hipertiroidismo |
| ENFERMEDADES GASTROINTESTINALES |
| Gastrectomía subtotal Síndromes de malabsorción Ictericia obstructiva crónica Cirrosis biliar primaria y otras cirrosis Alactasia |
| TRASTORNOS DE LA MÉDULA ÓSEA |
| Mieloma múltiple Linfoma Leucemia Anemias hemolíticas Mastocitosis sistémica Carcinoma diseminado |
| ENFERMEDADES DEL TEJIDO CONJUNTIVO |
| Osteogénesis imperfecta Síndrome de Ehlers-Danlos Síndrome de Marfan Homocistinuria |
| FÁRMACOS |
| Alcohol Heparina Glucocorticoides Tiroxina Anticonvulsivantes Agonistas de la hormona liberadora de gonadotropinas Ciclosporina Tacrolimús Quimioterapia Inhibidores selectivos de la recaptación de serotonina (?) Tiazolidinedionas Inhibidores de la bomba de protones |
| MISCELÁNEA |
| Inmovilización Artritis reumatoide Acidosis tubular renal |
Otras enfermedades sistémicas pueden producir osteoporosis (v. tabla 251-2 ). Los pacientes con trastornos hepatobiliares con frecuencia tienen osteoporosis y/u osteomalacia debido a la alteración de la absorción de vitamina D y al hiperparatiroidismo secundario. La enteropatía por gluten es una de las enfermedades hereditarias más frecuentes y los pacientes con frecuencia tienen una pérdida de masa ósea en la etapa adulta ( cap. 252 ). Estos pacientes a menudo tienen concentraciones bajas de 25-hidroxivitamina D y concentraciones muy elevadas de PTH con elevaciones modestas de la fosfatasa alcalina total. El diagnóstico definitivo se realiza con una biopsia del intestino delgado, aunque las concentraciones de transglutaminasa tisular pueden ser muy útiles en el cribado de individuos con pérdida de masa ósea. Los pacientes con trastornos sistémicos como el lupus eritematoso ( cap. 274 ), la esclerodermia ( cap. 275 ), la artritis reumatoide ( cap. 272 ) y la enfermedad mixta del tejido conjuntivo también pueden tener pérdida de masa ósea independientemente de si han sido tratados con corticoides. Esta forma de osteoporosis secundaria se produce con más probabilidad por la combinación de inmovilidad, malabsorción y la liberación de citocinas inflamatorias, tanto localmente como de forma sistémica, así como el empleo de medicamentos que pueden alterar el esqueleto, como la heparina, el etanol, la ciclosporina, el tacrolimús y los agentes anticonvulsivantes. La ingestión crónica de alcohol ( cap. 32 ) puede ser especialmente perjudicial para el esqueleto, dado que puede suprimir la función de los osteoblastos, aumentar la diferenciación de las células estromales hacia adipocitos y potenciar la resorción ósea. Muchos pacientes que padecen alcoholismo crónico sufren hipogonadismo (sea primario o secundario) y con frecuencia tienen concentraciones bajas de vitamina D. Los pacientes varones con hipercalciuria y/o cálculos renales también tienen riesgo de pérdida de masa ósea y fracturas osteoporóticas. La patogenia de esta relación no está del todo clara pero el hiperparatiroidismo secundario en pacientes con hipercalciuria potencia la resorción ósea y la pérdida gradual de hueso. Por último, la pérdida ósea inducida por fármacos es una causa importante de osteoporosis secundaria. Además de los glucocorticoides, el tratamiento crónico con heparina, algunos anticonvulsivantes, las tiazolidinedionas y algunos antipsicóticos de segunda generación pueden producir osteoporosis. Recientemente, se ha relacionado el uso de los inhibidores selectivos de la recaptación de serotonina (ISRS) de segunda generación y de inhibidores de la bomba de protones con pérdida de masa ósea y fracturas osteoporóticas en mujeres y varones de edad avanzada. Si se confirmase en ensayos clínicos prospectivos, estos agentes se convertirían en la causa más frecuente de osteoporosis secundaria.
Neoplasias
Las neoplasias metastásicas al esqueleto a veces se manifiestan como fracturas osteoporóticas o como lesiones líticas de significado incierto. Generalmente, estas lesiones tienen una localización atípica (p. ej., la parte media de la diáfisis de los huesos largos o la pelvis) y la causa subyacente con frecuencia es obvia. Se confunden con menor frecuencia con osteoporosis las lesiones osteoblásticas de las vértebras o los huesos largos. Sin embargo, los trastornos primarios hematopoyéticos y linfoproliferativos suelen ser insidiosos y pueden asociarse con pérdida de la masa ósea y con fracturas. El mieloma múltiple ( cap. 193 ) es el trastorno maligno hematológico más frecuente relacionado con osteoporosis, dado que los pacientes con esta enfermedad con frecuencia tienen osteopenia difusa, ocasionalmente con fracturas osteoporóticas clásicas de la columna vertebral o de los huesos largos. Contrariamente a otros procesos metastásicos del hueso, el mieloma múltiple se asocia con tasas muy elevadas de resorción ósea pero sin cambios ni supresión en la formación de hueso. Esta situación puede producir una pérdida ósea rápida. Las células plasmáticas liberan citocinas, en concreto TNF-α, IL-1 e IL-6, que estimulan la osteoclastogénesis. De forma simultánea, estas células producen Dickopf I y III, factores solubles que bloquean esta red establecida crítica de Wnt/LRP5/β-catenina. Por tanto, los pacientes tienen desacoplamientos importantes en la remodelación ósea, pérdida rápida de hueso y fracturas. Hoy en día, sigue en pie el debate sobre la relación de la osteoporosis con las gammapatías monoclonales de significado incierto (MGUS), aunque en estos pacientes se comunica con frecuencia la presencia de osteopenia. Otras causas de osteoporosis secundaria se enumeran en la tabla 251-2 .
Manifestaciones clínicas
Aunque la osteoporosis se considera con frecuencia una enfermedad silente, su presentación ha cambiado de forma drástica en las últimas dos décadas. Anteriormente, las formas más frecuentes de presentación eran fracturas vertebrales con o sin pérdida de altura. Hasta hace poco, las fracturas de cadera en pacientes ancianos, que pueden ser una manifestación final de la osteoporosis, con frecuencia eran consideradas traumáticas y no metabólicas. De forma similar, las fracturas de muñeca en mujeres posmenopáusicas precoces son indicación de signo de alarma de una osteoporosis subyacente. En el pasado eran tratadas por cirujanos ortopédicos sin tener en cuenta los procesos patológicos esqueléticos subyacentes. Sin embargo, estas tendencias empezaron a cambiar en la primera parte del siglo xxi , sobre todo con la disponibilidad del absorciómetro dual de energía de rayos X (DXA), el método de elección para medir la DMO. Hoy en día, la forma más frecuente de presentación de la osteoporosis es una medida baja de la DMO, realizada de forma rutinaria o con motivo de estudios preventivos. Dado que la masa ósea es sólo uno de los factores de riesgo de la osteoporosis, se deben tener en cuenta otras manifestaciones clínicas de esta enfermedad. La pérdida de más de 5 cm de altura es un marcador razonable de fracturas vertebrales previas. Los antecedentes clínicos de fracturas de muñeca o tobillo son otra indicación de osteoporosis subyacente y puede ser la primera manifestación de la enfermedad en mujeres jóvenes posmenopáusicas. Otra forma de presentación de la osteoporosis son las fracturas por compresión de la columna vertebral con un estrés mínimo. Estas fracturas producen un dolor importante en la zona lumbar o torácica baja que puede irradiarse a los costados o hacia la parte anterior. Un dolor agudo en la espalda, como una punzada, después de un traumatismo agudo suele ser incapacitante y con frecuencia requiere analgésicos opiáceos y se suele resolver en un período de semanas a meses a no ser que se produzca una nueva fractura. Los pacientes tienen una probabilidad aproximada del 20% de tener nuevas fracturas vertebrales en los primeros años tras una fractura de columna. Además, algunos pacientes sufren dolor lumbar crónico como resultado de una o más fracturas vertebrales. La pérdida de masa ósea por sí misma no produce dolor lumbar y deben plantearse otros diagnósticos en esta situación. La lordosis cervical y la cifosis dorsal son las manifestaciones clásicas de la «joroba de viuda» pero se observan con menor frecuencia en mujeres jóvenes. Las fracturas de cadera debidas a alteraciones en el cuello femoral, el trocánter o la zona cervical, generalmente se producen después de una caída. La dirección y la altura de la caída son elementos críticos para determinar el tipo de fractura de cadera, la cirugía subsiguiente y la discapacidad. Las fracturas de cadera pueden ser muy catabólicas, debido al traumatismo y a la cirugía importante ulterior. Estos factores, en combinación con la enfermedad subyacente, potencian la mortalidad por las fracturas de cadera en individuos ancianos hasta una tasa del 20% en el primer año.
La osteoporosis también puede ser diagnosticada por un radiólogo o por el médico de atención primaria a partir de radiografías simples como se muestra en la figura 251-4 . Con frecuencia, los pacientes tienen una pérdida obvia de masa ósea que provoca el término radiológico osteopenia, aunque en este estadio la DMO medida por DXA generalmente está por debajo de −2,5 DE. Las radiografías de columna pueden demostrar una cifosis, osteopenia y fracturas por compresión en las vértebras torácicas o lumbares. En la zona lumbar alta o torácica baja, que son las más vulnerables a los traumatismos, se visualizan con frecuencia fracturas por compresión. Con frecuencia se visualizan en las radiografías laterales de columna colapsos de elementos anteriores o posteriores; el acuñamiento anterior o la deformidad denominada «vértebra en pez» puede deberse al adelgazamiento de las placas subcondrales y a la expansión de los discos intervertebrales (v. fig. 251-4 ).
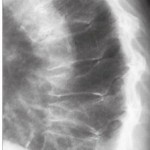
Figura 251-4
Radiografía que muestra radiolucencia, fracturas por compresión y cifosis en las vértebras de un paciente con osteoporosis.
La tomografía computarizada (TC) de la columna realizada por otros motivos puede detectar con frecuencia fracturas y puede utilizarse clínicamente para medir la densidad. La resonancia magnética (RM) se utiliza hoy en día con mayor frecuencia como instrumento diagnóstico; puede mostrar una fractura por compresión con o sin edema medular que provoca una señal brillante en las imágenes T1.
Las gammagrafías óseas con tecnecio-99m son muy sensibles para detectar fracturas y se utilizan para detectar fracturas de estrés en la pelvis, el fémur o la tibia. Sin embargo, debido a su elevada sensibilidad, esta prueba no es útil para el diagnóstico de osteoporosis. De hecho, es infrecuente que la gammagrafía sea la clave inicial de la osteoporosis y en el contexto de una gammagrafía positiva se deben plantear diagnósticos alternativos, incluida la enfermedad neoplásica.
Diagnóstico
Una fractura reciente por fragilidad de la columna, la cadera, la muñeca, el tobillo, el hombro o localizaciones apendiculares en mujeres posmenopáusicas o en varones debería conducir al diagnóstico de osteoporosis. Sin embargo, se deben excluir causas secundarias de esta enfermedad (como se ha mencionado anteriormente y enumerado en la tabla 251-2 ) antes de iniciar el tratamiento. De forma similar, dado que la OMS ha establecido que una DMO inferior a −2,5 DE en cualquier localización desde el valor normal en jóvenes cumple los criterios para el diagnóstico de osteoporosis, el diagnóstico puede realizarse a partir de resultados o medidas de densitometría. Sin embargo, este hallazgo debe ser interpretado con relación a la edad del paciente, la etnia, los antecedentes de fractura, los antecedentes familiares, las medicaciones previas, el momento de la menopausia y otras enfermedades concomitantes. Actualmente, basándose en los criterios de la OMS, la mayoría de los médicos realizan el diagnóstico de osteoporosis midiendo la densidad ósea con o sin marcadores bioquímicos de recambio óseo. Recientemente, la introducción por la OMS de la herramienta en internet FRAX ha convertido la predicción del riesgo de fracturas a largo plazo en una herramienta importante y fácil para el paciente y el profesional sanitario.
- Últimos artículos sobre Causas secundarias de pérdida ósea en el adulto
- Resultados sobre osteoporosis & Causas secundarias de pérdida ósea en el adulto
Medidas por absorciometría de energía dual con rayos X de la densidad mineral ósea
Las técnicas para medir la masa ósea son las siguientes: DXA de la columna vertebral, la cadera, el radio o todo el cuerpo; TC de la columna; ecografía del calcáneo o la muñeca; DXA del dedo; TC periférica cuantitativa de la muñeca o la tibia. Otras técnicas experimentales que están siendo evaluadas para medir el hueso trabecular o la calidad ósea son la RM del calcáneo y el radio, la RM virtual utilizando reconstrucciones computarizadas del hueso trabecular y la «TC extrema» con imágenes de muy alta resolución del radio. La técnica más popular, menos cara y más precisa es la DXA. Los resultados de las medidas de DXA se expresan tradicionalmente como puntuaciones T-score o Z-score . La T-score es el número de DE por debajo o por encima del cual la DMO del paciente difiere del pico de densidad ósea de un sujeto del mismo sexo y la misma etnia. La Z-score es el número de DE en el cual la densidad ósea del paciente difiere de la de un sujeto pareado por edad, sexo y etnia. No es sorprendente que exista una disparidad en la DMO absoluta de todo el cuerpo dentro del mismo sujeto. Esta disparidad puede atribuirse a la proporción relativa de hueso trabecular y cortical en localizaciones concretas. Por tanto, por ejemplo, la vértebra contiene un 85% de hueso trabecular, mientras que la diáfisis femoral o el cuello contienen principalmente hueso cortical. Diversos estudios han demostrado que casi un tercio de los sujetos tienen T-scores dispares de cadera y de columna. Este hallazgo se atribuye a las diferencias en la composición del esqueleto; en otras palabras, el hueso cortical, o la capa externa, es más delgado y se remodela con menor frecuencia, mientras que el hueso trabecular, que es un hueso espongiforme interno rodeado de elementos medulares, es metabólicamente más activo. La DXA integra ambos compartimentos esqueléticos como un área de medida. Sin embargo, dado que con frecuencia las distintas localizaciones esqueléticas difieren en composición y función, esta disparidad se observa con frecuencia. Además, los cambios relacionados con la edad difieren en ambos compartimentos óseos y sus determinantes genéticos pueden ser completamente diferentes. En general, se recomienda que la medida más baja de DMO en cualquier localización se emplee para evaluar el riesgo de fractura.
Las dos localizaciones esqueléticas más frecuentemente recomendadas para medir la DMO por técnica de DXA son la columna y la cadera. Para la columna, se pueden obtener DXA anteroposterior y lateral de columna, aunque la mayoría de los técnicos utiliza la anteroposterior de columna, que es un indicador más sensible de pérdida ósea precoz y una medida más precisa. Sin embargo, la DXA anteroposterior de columna puede mostrar con frecuencia una masa ósea elevada debida a incrementos en la artritis degenerativa, el colapso discal, las fracturas vertebrales y/o la calcificación de la aorta. Por tanto, en pacientes mayores de 65 años, es preferible realizar una medida de la DMO del cuello femoral o de la cadera. Ambos tienen una buena precisión, son fiables y no están artefactados por otros procesos en curso. Cualquier localización tiene un valor predictivo importante para fracturas ulteriores.
- Últimos artículos sobre Medidas por absorciometría de energía dual con rayos X de la densidad mineral ósea
- Resultados sobre osteoporosis & Medidas por absorciometría de energía dual con rayos X de la densidad mineral ósea
Otros instrumentos para medir la masa ósea
Están disponibles otros medios para medir la DMO, y cada uno aporta T-scores equivalentes, aunque no pueden intercambiarse fácilmente entre las distintas tecnologías. La TC cuantitativa de las vértebras aporta medidas volumétricas reales de la masa ósea (mg/cm 3 ), puede detectar una pérdida ósea precoz, es fiable y está disponible en muchos centros. Sin embargo, su reproducibilidad no es tan buena como la DXA y las puntuaciones T-score pueden ser bastante dispares de las medidas por DXA. Además, se produce una mayor radiación con la TC que con la DXA, y la TC requiere más tiempo. La ecografía de partes periféricas tiene la ventaja de la portabilidad y la facilidad de la técnica y es una técnica que permite al médico predecir fracturas; sin embargo, los parámetros utilizados para medir la transmisión de sonido no cambian mucho con la edad, o con el tratamiento, por lo que es un instrumento difícil para su empleo en el seguimiento. La TC cuantitativa periférica es cara pero fiable; tiene una mayor exposición a radiación pero aporta información sobre los elementos de hueso cortical y trabecular. Con esta técnica tenemos menos datos disponibles sobre el riesgo de fractura, por lo que es principalmente una técnica de investigación.
En resumen, la DXA aporta el instrumento más fiable y preciso para evaluar el riesgo de fractura. La medida con DXA, combinada con la edad, los antecedentes de fractura previa y los antecedentes familiares, aporta al médico la valoración más fiable del riesgo osteoporótico. Para el seguimiento, las medidas de DMO con DXA son preferibles a otras tecnologías por sus menores errores de precisión y su mayor reproducibilidad.
- Últimos artículos sobre Otros instrumentos para medi r la masa ósea
- Resultados sobre osteoporosis & Otros instrumentos para medi r la masa ósea
Evaluación del riesgo con FRAX
Desde la introducción generalizada de mediciones de la densidad ósea está claro que la DMO aislada no es suficiente para definir el riesgo global de fractura y que es esencial tener en cuenta los factores de riesgo clínicos. A menudo, se realiza en el centro de asistencia utilizando la edad (>65 años), las fracturas previas y los antecedentes familiares. Sin embargo, esta combinación ofrece una estimación del riesgo a 10 años, que los médicos utilizan con frecuencia para evaluar otras afecciones, como el infarto de miocardio. Por ello, la OMS, en colaboración con fundaciones para la osteoporosis internacionales, desarrolló una herramienta virtual, FRAX, que se puede utilizar al lado del paciente para determinar su riesgo de fractura a 10 años. En cualquier ordenador, se introduce en un cuadro la DMO determinada por DXA junto con la edad, la altura, el sexo, el país y las respuestas a preguntas sobre la historia familiar, el uso de glucocorticoides o alcohol, las fracturas previas y la pérdida de peso. A continuación se calcula el riesgo de fractura a 10 años en porcentaje para una fractura importante (es decir, vertebral, cadera, muñeca, húmero) así como el riesgo aislado de fractura de cadera. Las directrices actuales sugieren que los individuos de alto riesgo son aquéllos con un riesgo a 10 años de fractura de cadera superior al 3% y con riesgo de fractura osteoporótica importante superior al 20%.
La FRAX como herramienta clínica ha sido ampliamente alabada, y su uso ha aumentado de una forma importante desde su introducción en 2007. Su fortaleza reside en la posibilidad de realizar la evaluación del riesgo directamente al lado del paciente, ser una evaluación específica por país (p. ej., EE.UU. frente a Reino Unido frente a Francia), las revisiones recientes que incorporan nuevos conjuntos de datos que ofrecen incidencias de fracturas para EE.UU. más actualizadas y la facilidad de uso. Existen preocupaciones sobre varias limitaciones, entre las que se encuentra que para el riesgo de fractura sólo se introduce la DMO. El FRAX no se debe utilizar en pacientes que ya están recibiendo tratamiento; y, en algunas poblaciones, el riesgo está sobreestimado, particularmente en la mujer posmenopáusica más joven. No obstante, la evaluación del riesgo de fractura ofrece una estimación fiable tanto para el paciente como para el profesional sanitario y es preferible a una única medida de la DMO para establecer el riesgo.
- Últimos artículos sobre Evaluación del riesgo con FRAX
- Resultados sobre osteoporosis & Evaluación del riesgo con FRAX
Marcadores biológicos: marcadores bioquímicos del recambio óseo
Desde la mitad de la década de 1980 se han desarrollado nuevos métodos para medir la rotura ósea y la síntesis de productos. Anteriormente, se utilizaban dos marcadores urinarios, el calcio y la hidroxiprolina, para evaluar la resorción ósea; ambos eran inespecíficos y con poca precisión. Posteriormente, diversos marcadores bioquímicos séricos y en orina se han perfeccionado y estudiado en amplios ensayos clínicos que se encuentran disponibles para uso clínico actualmente. Los marcadores de resorción ósea mediados por osteoclastos incluyen la piridinolina y la desoxipiridinolina urinarias, así como las uniones de péptidos C terminal y N terminal de colágeno de tipo I. Estos últimos pueden medirse tanto en orina como en suero. Los marcadores de formación ósea mediada por osteoblastos incluyen la fosfatasa alcalina específica del hueso, la osteocalcina, el propéptido amino-terminal de procolágeno de tipo I y el propéptido carboxi-terminal de procolágeno de tipo I. Los aumentos de los marcadores de formación o reabsorción o de ambos implican una remodelación acelerada. Por ejemplo, inmediatamente después de que cese la producción de estrógenos, incrementan de forma muy importante los marcadores de formación y resorción ósea. De forma similar, en etapas tardías de la vida, y durante estados de hiperparatiroidismo secundario, estos marcadores pueden estar muy elevados. Además, los fármacos antirresortivos, como los estrógenos o los bifosfonatos, disminuyen de forma significativa las concentraciones urinarias y circulantes de estos marcadores. Los estudios longitudinales y transversales han demostrado que las concentraciones elevadas de marcadores de recambio óseo predicen fracturas en mujeres ancianas. Estos marcadores son independientes del riesgo de DMO, un hallazgo que sugiere que el recambio óseo acelerado por sí mismo es un riesgo de fractura. Estos índices de recambio óseo proporcionan una estimación actual del estado del esqueleto, mientras que las medidas de la densidad ósea son estequiométricas y reflejan todos los sucesos que contribuyen a la medida.
Además de la posibilidad que ofrecen de definir el riesgo de fractura, diversos grupos han demostrado que la supresión de los marcadores de recambio con bifosfonatos puede predecir la reducción del riesgo de fractura en mujeres posmenopáusicas de edad avanzada. Sin embargo, el empleo de estos marcadores en la práctica clínica ha sido decepcionante por diversos motivos. En primer lugar, la variabilidad en las medidas individuales, sobre todo en los estudios urinarios, es bastante elevada. Por tanto, incluso una medida aislada tiene un nivel significativo de error; debido a esta variabilidad, el seguimiento para evaluar los cambios con respecto al estado basal es con frecuencia muy confuso. En segundo lugar, la mayoría de las mujeres tiene valores de marcadores de recambio dentro del rango normal, lo cual dificulta la interpretación. En tercer lugar, el número de mujeres mayores con un recambio óseo elevado probablemente ha sido sobreestimado, sobre todo en los períodos posmenopáusicos precoces. Estos aspectos hacen que haya poco entusiasmo en estas pruebas sanguíneas o urinarias para determinar el riesgo y ayudar al manejo una vez que el tratamiento ha sido establecido. De forma ocasional, estas pruebas pueden ser útiles: en mujeres jóvenes que tienen una menopausia prematura debido a la quimioterapia, por ejemplo, el conocer no sólo la DMO sino también la tasa de recambio óseo podría ayudar en el tratamiento de su enfermedad con terapia antirresortiva más intensa o con un enfoque más medido utilizando calcio y vitamina D. No está recomendado determinar de forma rutinaria estos marcadores para evaluar el cumplimiento de los tratamientos antirresortivos.
- Últimos artículos sobre Marcadores biológicos: marcadores bioquímicos del recambio óseo
- Resultados sobre osteoporosis & Marcadores biológicos: marcadores bioquímicos del recambio óseo
Osteoporosis inducida por glucocorticoides
La causa más frecuente de osteoporosis secundaria es la inducida por glucocorticoides. Esto se debe con frecuencia a dosis farmacológicas de corticoides empleados en el tratamiento de enfermedades inflamatorias o autoinmunitarias. Generalmente, se considera que los glucocorticoides ( cap. 34 ) tienen un efecto dependiente de la dosis sobre el hueso, es decir, que la duración larga y las dosis altas de corticoides tienen más probabilidades de producir pérdida ósea y fracturas. Sin embargo, existen claramente unos grupos de pacientes que son más o menos sensibles a los efectos óseos de las dosis altas de glucocorticoides. Como regla clínica general, aquellos sujetos con un aspecto cushingoide y con una redistribución de la grasa corporal casi siempre tienen una pérdida de masa ósea y/o fracturas.
Los efectos de los glucocorticoides sobre el esqueleto son multifacéticos y son especialmente devastadores, dado que estos fármacos producen un desacoplamiento de la unidad de remodelación ósea. Aparte de los efectos supresores indirectos de los glucocorticoides sobre el eje hipotalámico-gonadal, la inhibición de la absorción de calcio en el intestino, las altas dosis de corticoides pueden estimular la osteoclastogénesis, aumentar la producción de RANKL y disminuir la OPG. Esta situación provoca unas tasas elevadas de resorción ósea. Además, los glucocorticoides también tienen un fuerte efecto negativo sobre la formación de hueso suprimiendo la expresión de IGF-I en las células óseas y provocando un cambio de las células estromales medulares hacia la línea adiposa, en lugar de una diferenciación hacia osteoblastos. Se piensa que al igual que la redistribución de grasa es una característica clínica del síndrome de Cushing en la zona supraclavicular y mediastínica, la mayor adiposidad en la médula ósea es un rasgo característico, casi seguro debido al incremento de la diferenciación de células estromales hacia adipocitos. La resistencia ósea está muy alterada debido al desacoplamiento en la reestructuración y la pérdida de hueso puede ser rápida en cortos períodos de tiempo, sobre todo con dosis altas de glucocorticoides. Aunque no existe un verdadero efecto dependiente de la dosis en la resorción ósea, se cree que la prednisona a dosis tan bajas como 5 mg/día puede aumentar el riesgo de fractura. Además, en este síndrome, la DMO basal no es predictiva de fracturas y puede ser normal con frecuencia, incluso en presencia de una resorción en curso y de fracturas recurrentes. El hueso trabecular es el que más sufre en este síndrome, y la DXA de columna es el indicador más sensible de la pérdida ósea. Los marcadores bioquímicos de recambio óseo no son útiles en el tratamiento de estos pacientes.
El tratamiento de la pérdida de hueso inducida por corticoides se centra en tratar la enfermedad subyacente y/o reducir la dosis de glucocorticoides al nivel mínimo posible. Aparte de esto, diversas intervenciones han demostrado retardar la pérdida ósea y prevenir las fracturas. La ingestión adecuada de calcio y vitamina D es crítica en todo paciente que recibe glucocorticoides. Sin embargo, estas medidas por sí solas no son suficientes. Tres bifosfonatos han demostrado ser eficaces en la osteoporosis inducida por glucocorticoides: etidronato, alendronato
y risedronato, y hoy en día están considerados la piedra angular del tratamiento de esta enfermedad. Estos fármacos se administran bien semanalmente o cíclicamente para prevenir la pérdida ósea y para reducir el riesgo de fracturas. Algunos datos anecdóticos apoyan el uso de esteroides gonadales en esta situación, pero los bifosfonatos son claramente superiores. En un ensayo clínico aleatorizado, la PTH sintética (teriparatida, 20 mg diarios subcutáneos durante 18 meses) aumentó de forma significativa la densidad de masa ósea de la cadera y vertebral y redujo las fracturas no vertebrales nuevas (del 7,2% al 3,4%) pero no otras fracturas, en comparación con el alendronato
. Se necesitan más estudios para establecer su eficacia en esta enfermedad, sobre todo porque el hiperparatiroidismo secundario es frecuente en la osteoporosis inducida por corticoides.
Estrategias futuras
El denosumab, un anticuerpo sintético anti-RANKL que actúa igual que la OPG, previene la pérdida de hueso en mujeres con enfermedad grave y, en ensayos clínicos aleatorizados controlados por placebo de gran tamaño, redujo las fracturas de cadera, vertebrales y no vertebrales administrado como inyección subcutánea única (60 mg) cada 6 meses. Este fármaco no se asocia a osteonecrosis de la mandíbula, pero existe una incidencia de celulitis de las extremidades inferiores tres veces superior con el fármaco que con el placebo. Actualmente, denosumab no está autorizado por la FDA. La proteína relacionada con la PTH (PTHrp), un péptido estructuralmente similar a la PTH, se une al mismo receptor, es responsable en algunos casos de la hipercalcemia por neoplasias y ha demostrado tener ciertas propiedades anabólicas cuando se administra de forma intermitente. Aún no está autorizada por la FDA para el tratamiento de la osteoporosis.
- Últimos artículos sobre Osteoporosis inducida por glucocorticoides
- Resultados sobre osteoporosis & Osteoporosis inducida por glucocorticoides
Definición
La osteoporosis es un trastorno caracterizado por una fragilidad esquelética aumentada como resultado de una disminución de la cantidad y la calidad del hueso. Los síntomas clínicos de esta enfermedad pueden incluir dolor de espalda, pérdida de altura y/o antecedentes de fracturas. La densidad mineral ósea (DMO), que puede ser determinada con diversas técnicas, con frecuencia está muy disminuida en pacientes osteoporóticos con fracturas. La Organización Mundial de la Salud (OMS) define la osteoporosis como una entidad en la cual la DMO es menor de −2,5 desviaciones estándar (DE) por debajo del pico de masa ósea (es decir, una puntuación T [t-score] medida como unidades de DE por debajo de la media estándar para las mujeres de 35 años). Sin embargo, diversos estudios observacionales amplios han demostrado que las fracturas osteoporóticas pueden producirse en un amplio espectro de DMO. Estos sucesos probablemente estén relacionados con una calidad ósea alterada, como resultado de cambios de la microarquitectura del esqueleto trabecular y cortical. Los determinantes cualitativos de las fracturas osteoporóticas incluyen perforaciones trabeculares, microfisuras, defectos de mineralización, tamaño del hueso y/o recambio óseo acelerado ( fig. 251-1 ). Desgraciadamente, la mayoría de los cambios cualitativos del esqueleto no pueden evaluarse con medidas clínicas, aunque influyan en gran parte en el riesgo general de fractura. Recientemente, la introducción de la tomografía computarizada (TC) de extrema resolución y de determinaciones en la TC más refinadas han permitido a los investigadores medir de forma precisa el tamaño, el número y la forma de las trabéculas, aunque hasta la fecha estas nuevas herramientas no aumentan de forma marcada la capacidad de predicción de fracturas. Por tanto, aunque una DMO baja defina la osteoporosis, este diagnóstico no debería excluirse en individuos susceptibles, sobre todo aquéllos con antecedentes de una fractura por impacto bajo. Finalmente, aunque la OMS define la osteopenia como una entidad en la cual la puntuación T se encuentra entre −1,0 y −2,5, lo que sitúa al individuo en un mayor riesgo de fractura, el significado clínico de este término es incierto. La introducción de FRAX, una herramienta en internet, que sopesa los factores clínicos de riesgo con la DMO de la cadera, puede ofrecer una mejor comprensión sobre el riesgo de fractura a largo plazo en los sujetos con baja masa ósea. En resumen, la DMO baja supone un factor de riesgo importante para las fracturas ulteriores, pero no existe un umbral de DMO por encima o por debajo del cual ocurran las fracturas. Otros factores de riesgo, como los antecedentes de fracturas previas, la edad superior a 65 años, los antecedentes familiares intensos y una pérdida importante de peso reciente, deben ser tenidos en cuenta.
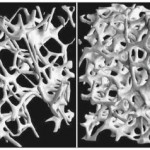
Figura 251-1
Imágenes de microtomografía computarizada del hueso trabecular de una vértebra en un sujeto con osteoporosis (izquierda) y en una mujer sana de la misma edad (derecha).
Biología
Pico de masa ósea
La adquisición de una masa de hueso máxima se produce entre los 12 y los 15 años de edad, aunque depende en gran medida del sexo (es decir, las chicas alcanzan el pico antes que los chicos) y del tipo de hueso (es decir, trabecular frente a cortical). Durante este tiempo, se produce un tremendo incremento de la masa ósea como resultado del crecimiento y la remodelación del esqueleto que favorece la formación de hueso sobre la resorción. Las liberaciones puberales de esteroides gonadales y hormona de crecimiento son críticas para este incremento drástico en la masa ósea que se produce en la adolescencia. Los estudios longitudinales sugieren que diversos factores regulan el pico de densidad ósea, incluida la ingesta dietética de nutrientes específicos, la actividad física y, lo más importante, los determinantes genéticos ( tabla 251-1 ). Esta visión fue establecida en diversas vías, tanto en modelos humanos como animales. Las hijas de madres con osteoporosis grave tienen una DMO baja. Los gemelos monocigóticos tienen una mayor concordancia en la masa ósea que los gemelos dicigóticos y las cepas consanguíneas de ratones difieren significativamente en el pico de DMO. Sin embargo, a pesar de los esfuerzos importantes realizados en la década pasada para identificar los determinantes hereditarios que influyen en la masa ósea, se ha realizado poco progreso. Las diferencias polimórficas en los genes candidatos más prometedores, incluidos los genes de la vitamina D y de los receptores de estrógenos, del factor de crecimiento de tipo insulina-I (IGF-I), la hormona paratiroidea (PTH), el colágeno A1a, Lrp5, y otros se asocian con la masa ósea. Pero estos determinantes genéticos sólo contribuyen individualmente al 1%-3% de las variaciones en la DMO. Es probable, aunque aún no se ha demostrado, que los polimorfismos de nucleótidos en múltiples genes contribuyan más a la masa ósea que los cambios de genes únicos.
Tabla 251-1
Factores que pueden afectar el pico de masa ósea
| Sexo Raza Factores genéticos Esteroides gonadales Hormona de crecimiento Momento de la pubertad Ingesta de calcio Ejercicio |
Formación ósea
Los investigadores han descubierto dos nuevos patrones en los osteoblastos que están regulados genéticamente y afectan la tasa de formación de hueso. Estos son: 1) el sistema de señalización Wnt/Lrp5/β-catenina y 2) la vía de la lipooxigenasa. En el primero, las mutaciones activadoras de la proteína 5 del receptor de lipoproteína de baja densidad (LRP5) producen una masa ósea elevada, mientras que las mutaciones inactivadoras producen un síndrome de osteoporosis y seudogangliomas, una enfermedad relacionada con pérdida de masa ósea en los niños. El patrón de señalización establecido LRP5 es estimulado por ligandos Wnt y provoca directamente una mayor proliferación y diferenciación de los osteoblastos. En el segundo sistema, dos enzimas críticas determinan cuándo y cómo las células estromales evolucionan hacia células grasas o células óseas: la 12,15-lipooxigenasa ( 12LO o Alox 12,15 ) produce prostaglandinas y otros ligandos endógenos que se unen al receptor nuclear receptor activador del proliferador de peroxisomas γ (PPARG) que estimula la diferenciación hacia adipocito; y la 5′LO, o Alox 5, produce leucotrienos que también activan el PPARG mediante la generación de prostaglandina J2. Los polimorfismos en estos dos genes en ratones y en humanos se han asociado con diferencias en el pico de masa ósea. Los estudios en gemelos han demostrado que la regulación genética del pico de masa ósea puede ser modificada por factores hormonales y ambientales. En concreto, la secreción adecuada y a tiempo de los esteroides sexuales, la ingesta nutricional equilibrada y la actividad física pueden optimizar el pico de DMO incluso en personas con predisposición genética a masa ósea baja. Es probable que las perturbaciones en la adquisición del pico óseo contribuyan a la osteoporosis en una etapa más tardía de la vida. Por ejemplo, los hombres con pubertad retardada constitucional tienen menor DMO que sus iguales de 30 a 40 años que tuvieron la pubertad en la edad adecuada. Las mujeres con anorexia nerviosa durante la adolescencia tienen una DMO significativamente menor en el momento de la menopausia que las adolescentes sanas que no desarrollan amenorrea. Las mujeres con menarquia retardada también tienen una menor DMO en la edad adulta que las mujeres con comienzo normal de la menarquia. Un área de controversia es si las fracturas en la infancia son un signo de osteoporosis futura. Al menos dos estudios han demostrado que las fracturas radiales en los adolescentes se asocian con una menor área de densidad ósea y una zona de hueso cortical disminuido en comparación con los hallazgos en niños que no tienen fracturas. Estos determinantes podrían predisponer a los niños a fracturas con impactos relativamente bajos y pueden ser una indicación de un riesgo futuro, aunque se precisan más estudios. Es interesante destacar que la obesidad en los niños es un factor de riesgo de fracturas del radio en el futuro.
Biopatología
La DMO en el adulto está determinada por la adquisición del pico de masa ósea durante la adolescencia y por el grado de pérdida ósea subsecuente durante toda la vida ( fig. 251-2 ). Estos dos procesos están regulados a nivel de la unidad de remodelación ósea, que está formada por osteoblastos formadores de hueso, osteoclastos resorbedores de hueso y osteocitos incluidos en la profundidad de la cortical capaces de detectar las fuerzas gravitacionales. La secuencia de remodelación está estrechamente orquestada a varios niveles por la interacción de factores genéticos, medioambientales y hormonales ( cap. 250 ). Incluso pequeños cambios en la formación ósea o en la resorción ósea pueden dar lugar a pérdida ósea o a alteración de la capacidad de alcanzar el pico de masa ósea durante la adolescencia. Aunque las fracturas osteoporóticas se producen inevitablemente como resultado de traumatismos, mayores o menores, en un hueso con una reducción de la cantidad o calidad del hueso, existe una fuerte relación inversa entre la DMO y las fracturas. Por tanto, los cambios en la remodelación que pueden dar lugar a una menor masa ósea son factores importantes al determinar el riesgo global de osteoporosis.
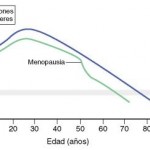
Figura 251-2
Densidad mineral del hueso cortical frente a edad en varones y mujeres.
Las mujeres tienen un pico inferior de densidad de hueso cortical en comparación con los varones y experimentan un período de pérdida rápida de hueso durante la menopausia, alcanzando el umbral de fractura (el nivel de densidad ósea en el cual el riesgo de presentación de fracturas osteoporóticas comienza a aumentar) antes que los varones.
La pérdida de hueso se produce cuando la unidad de remodelación ósea está desacoplada y la resorción excede la formación. El momento de pérdida ósea es un determinante crítico de un riesgo futuro de fractura. Por ejemplo, la pérdida rápida de hueso en personas ancianas les sitúa en un riesgo muy alto de fractura, independientemente de la DMO. A la inversa, el recambio óseo acelerado en un período corto de tiempo (como el relacionado con un exceso transitorio de corticoides en la edad adulta joven) puede provocar cambios reversibles en la masa ósea. Una vez que el suceso desencadenante (p. ej., tumor hipofisario) ha pasado o que se han interrumpido los tratamientos, el riesgo de fractura vuelve a la línea basal, y la DMO se restablece. Sin embargo, la pérdida de hueso también puede ser incesante, sobre todo en mujeres posmenopáusicas, en las cuales la privación de estrógenos produce un incremento importante de la actividad osteoclástica y un alto grado de remodelación. Aunque la unidad multicelular básica se encuentra estrechamente acoplada, la resorción rápida de hueso durante períodos prolongados produce un desequilibrio, dado que la formación de hueso no puede mantenerse en la misma tasa acelerada que la resorción. Durante los primeros pocos años de la menopausia (y posiblemente durante las fases tardías de la menopausia), al disminuir precipitadamente las concentraciones de estrógenos, se produce primero una pérdida del hueso trabecular. Esto se continúa con un adelgazamiento cortical. Ambas condiciones son el resultado de un desacoplamiento entre la resorción y la formación. Resulta sorprendente que durante la pérdida ósea en el adulto, se produce la expansión perióstica en un intento de conservar la resistencia ósea.
Durante la menopausia, los promedios de pérdida de hueso son de alrededor del 1% por año, pero en algunas mujeres la pérdida de DMO en la columna vertebral puede ser de hasta el 5% por año. Actualmente, es imposible identificar a estas mujeres de forma prospectiva. Además, la menopausia prematura, la disfunción ovárica inducida por quimioterapia y/o la amenorrea relacionada con ejercicio físico intenso producen tasas de resorción ósea incluso mayores que no pueden compensarse con la formación de hueso. Sin embargo, existe una tremenda heterogeneidad en la respuesta a la privación de estrógenos entre las mujeres posmenopáusicas. Unas pocas mujeres, en sus primeros años de la menopausia, pueden perder hueso a una tasa del 2% al 4% por año. Incluso entre las «rápidamente perdedoras» esto se vuelve más lento a lo largo del tiempo. La sustitución de estrógenos previene la pérdida ósea posmenopáusica incluso entre las «consumidoras rápidas», aunque la popularidad de este tipo de prevención ha disminuido en los años siguientes a la publicación del Women’s Health Initiative (WHI).
Pérdida ósea en personas ancianas
En la última etapa de la vida, sobre todo en la octava y novena décadas, la pérdida de hueso puede acelerarse de forma intensa. Diversos mecanismos potenciales son responsables de este cambio. En primer lugar, y de forma principal, los sujetos ancianos generalmente disminuyen la ingesta de vitamina D y calcio, además, tienen una menor exposición al sol. Este hallazgo, junto con una menor capacidad para generar previtamina D en la piel, produce un hiperparatiroidismo secundario y potencia la resorción ósea. Hay que destacar que más del 50% de las mujeres mayores de 70 años y que viven en latitudes norteñas tienen concentraciones insuficientes o deficientes de vitamina D (es decir, 25-hidroxivitamina D sérica <20 ng/ml). Otros factores también desempeñan un papel en el recambio óseo acelerado en la senectud. Las concentraciones aumentadas de homocisteína pueden potenciar la resorción ósea o pueden alterar la naturaleza de las especies reactivas de oxígeno dentro del ambiente óseo. Las citocinas inflamatorias, como la interleucina 6 (IL-6) y el factor de necrosis tumoral (TNF), también aumentan con la edad y pueden estimular el recambio óseo.
El desacoplamiento de la unidad remodeladora de hueso en una persona anciana puede asociarse con una alteración en la formación de hueso, dado que la función y el número de osteoblastos disminuyen con la edad. Estos cambios pueden relacionarse con concentraciones bajas de IGF-I circulante y/o esquelética o con otros factores tróficos que potencian la supervivencia de los osteoblastos o estimulan el reclutamiento de las células estromales. Las alteraciones en la asignación de estirpe de las células estromales pueden dar lugar a un aumento de la adipogénesis de la médula ósea a expensas de la diferenciación de los osteoblastos. El proceso de infiltración grasa de la médula ósea, especialmente en las vértebras de los individuos de edad avanzada, se debe en parte a un aumento relacionado con la edad de la activación del PPARG, un receptor nuclear y factor de transcripción esencial para la diferenciación de los adipocitos. Algunos fármacos pueden aumentar la activación del PPARG, entre éstos las tiazolidinedionas (p. ej., rosiglitazona y pioglitazona) y los glucocorticoides. Resulta interesante destacar que la activación del PPARG también puede estimular el desarrollo de nuevos osteoclastos, lo que da lugar a un importante desajuste entre la reabsorción y la formación. Como resultado de la alteración de la función osteoblástica, el déficit de la reestructuración se hace más pronunciado, sobre todo en situaciones de mayor resorción ósea. Independientemente de la causa de la pérdida ósea con la edad, los estrógenos y otras terapias antirresortivas son eficaces en la inhibición de la resorción ósea y en restablecer el equilibrio en las unidades remodeladoras del hueso, de forma que los dos procesos vuelven a estar acoplados.
- Últimos artículos sobre Pérdida ósea en personas ancianas
- Resultados sobre osteoporosis & Pérdida ósea en personas ancianas
Mecanismos moleculares y celulares en la remodelación normal
Para comprender mejor los mecanismos fisiopatológicos de la pérdida ósea es necesario definir los sucesos moleculares y celulares clave que se producen durante la reestructuración normal en adultos. Las células estromales mesenquimales, o células precursoras de osteoblastos, sufren una serie de estadios de diferenciación que culminan en un osteoblasto maduro capaz de asentar la matriz y segregar factores de crecimiento. Estas células, como se ha comentado previamente, son multipotenciales y, bajo la influencia de diversos factores, se pueden convertir en adipocitos, células musculares, condrocitos u osteoblastos. El destino último de las células estromales es un determinante crítico de la remodelación normal. Durante estos estadios de diferenciación, las células estromales liberan una serie de citocinas que se dirigen a los progenitores de osteoclastos provocando la diferenciación de células multinucleadas desde la línea macrofágica. Una vez que estas células se convierten en osteoclastos, tienen la capacidad de producir resorción ósea segregando protones y enzimas que disuelven la matriz ósea. Dentro de la matriz se encuentran diversos factores tróficos clave activados por la disolución de hueso; una vez que se introducen en el medio óseo, las células de la línea osteoblástica son forzadas a la diferenciación. De esta forma, la resorción ósea está acoplada a la formación ósea.
Diversas citocinas, incluida IL-1, IL-6, TNF, el factor nuclear activador del receptor κB (RANKL), y la osteoprotegerina (OPG), un receptor señuelo soluble para el RANKL, son segregadas por los preosteoblastos durante su proceso de diferenciación. El RANKL se expresa en la superficie de los precursores de osteoblastos, y su receptor RANK se encuentra en la superficie de los osteoclastos, un acoplamiento adecuado que permite de hecho la interacción célula a célula ( fig. 251-3 ). La unión del RANKL al RANK en presencia de concentraciones permisivas de otra citocina, el factor estimulador de colonias de macrófagos, estimula la diferenciación de los osteoclastos hacia células resorbedoras de hueso maduras. Por el contrario, la OPG, una proteína circulante también producida por las células estromales, puede unirse a RANKL e impedir su unión al RANK reduciendo de esta forma la osteoclastogénesis.
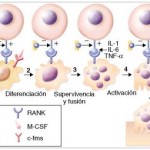
Figura 251-3
Regulación del desarrollo de los osteoclastos por el ligando del receptor activador del factor nuclear κB (RANKL), el receptor activador del factor nuclear κB (RANK) y la osteoprotegerina (OPG)
. c-fms = receptor para M-CSF; IL = interleucina; M-CSF = factor estimulador de colonias de macrófagos; TNF-α = factor de necrosis tumoral α.
(De Hofbaurer LC, Heufelder AE. The role of receptor activator of nuclear factor-κ ligand and osteoprotegerin in the pathogenesis and treatment of metabolic bone diseases. J Clin Endocrinol Metab . 2000;85:2355-2363.)
Patogénesis
- Últimos artículos sobre Mecanismos moleculares y celulares en la remodelación normal
- Resultados sobre osteoporosis & Mecanismos moleculares y celulares en la remodelación normal
Mecanismos celulares y moleculares de la pérdida ósea
La osteoporosis se produce por un desequilibro en la remodelación ósea. Los cambios en el recambio óseo pueden ser debidos a diversos factores que se dirigen a los osteoblastos y a los osteoclastos y dan lugar a una mayor resorción que formación. Por ejemplo, la disminución de los niveles de estrógenos durante la menopausia o tras la ooforectomía da lugar a una regulación al alza de todas las citocinas estromales, especialmente el RANKL. Por el contrario, existe una supresión de la secrección de la OPG. Este escenario da lugar a una mayor osteoclastogénesis y una resorción ósea acelerada. La formación ósea está acoplada a la resorción, por lo que se activa toda la unidad de remodelación. La resorción ósea es un proceso rápido, en el que los osteoclastos tardan unas 2 semanas en unirse y reabsorber la matriz. La formación es mucho más pausada, lo que significa que con la liberación de citocinas solubles se produce inmediatamente un desequilibrio en la remodelación, y esto favorece la resorción ósea. Al final, este desequilibrio conduce a un aumento de la destrucción del colágeno y la matriz ósea y a una incapacidad de emparejar esta pérdida con un aumento de la formación. La administración de estrógenos puede evitar la pérdida ósea al aumentar la producción de OPG así como mediante la supresión de la expresión del RANKL. Otros factores sistémicos y locales pueden producir un desequilibrio de la remodelación. Los elevados niveles de PTH durante largos períodos pueden estimular la expresión del RANKL y producir pérdida ósea. El exceso de glucocorticoides por administración exógena de esteroides o por enfermedad de Cushing también estimula la producción del RANKL y además produce un desplazamiento de la diferenciación de las células estromales desde la estirpe osteoblástica hacia la adipogénesis. La inmovilización suprime la formación ósea y aumenta la resorción ósea. El envejecimiento en general conduce a una reducción en varios factores tróficos osteoblásticos como IGF-I, así como un aumento de la activación del PPARG y estos cambios pueden alterar la velocidad de neoformación ósea.
- Últimos artículos sobre Mecanismos celulares y moleculares de la pérdida ósea
- Resultados sobre osteoporosis & Mecanismos celulares y moleculares de la pérdida ósea
Densitometría ósea
Están disponibles diversas técnicas para medir la DMO (es decir, medidas bidimensionales expresadas como g/cm 2 ) en el esqueleto axial y apendicular. Múltiples estudios prospectivos han demostrado de forma convincente que una DMO baja en cualquier localización (es decir, cadera, columna, radio, cuerpo total, calcáneo) predice fracturas osteoporóticas subsiguientes, ya sea en la misma zona o en otra localización. En general, independientemente de la tecnología, por cada 1 DE por debajo del valor normal joven (es decir, T-score ), el riesgo de fracturas osteoporóticas futuras aumenta alrededor del 50%. Sin embargo, las medidas en localizaciones concretas, por ejemplo la DMO de columna, generalmente predicen fracturas de columna mejor que la DMO de cadera. Debido a esta relación inversa entre riesgo de fractura y DMO, existe una razón importante para medir la masa ósea al menos una vez en toda mujer posmenopáusica.
Evaluación diagnóstica
El diagnóstico de osteoporosis generalmente se realiza con medidas de la masa ósea y/o antecedentes de fracturas osteoporóticas previas. Se deben excluir las causas secundarias de osteoporosis y se debe realizar un seguimiento para asegurarse de que la enfermedad no es rápidamente progresiva. Está indicado realizar análisis rutinarios de función renal y tiroidea. Se recomienda realizar una medida sérica de 25-hidroxivitamina D en individuos ancianos, sobre todo en las latitudes del norte, debido a que estas deficiencias pueden corregirse con suplementos de vitamina D. En el momento actual, la DXA representa el mejor instrumento para evaluar el riesgo global de fracturas y determinar la evolución con el tratamiento. Los marcadores bioquímicos pueden ser útiles en contadas ocasiones.
Plan de tratamiento
Un plan de tratamiento global para la osteoporosis incluye el diagnóstico de aquellas personas con mayor riesgo, excluyendo las causas secundarias de una DMO baja, y la selección del tratamiento adecuado. La toma de decisión debe tener en cuenta diversas salvedades. En primer lugar, el tratamiento de la osteoporosis puede disminuir el riesgo de fractura hasta un 50%, pero algunas mujeres continuarán teniendo fracturas a pesar del tratamiento. La identificación de estas mujeres con un riesgo importante de enfermedad progresiva es indispensable. En segundo lugar, las intervenciones farmacológicas y en el cambio de estilo de vida son compromisos duraderos, por lo que el coste, el cumplimiento y la seguridad deberían ser tenidos en cuenta en las decisiones terapéuticas. Los estudios sugieren que incluso con la terapia semanal con bifosfonatos, más del 40% de los sujetos tratados no continúa con el tratamiento más allá de 1 año. En tercer lugar, no es infrecuente que mujeres con T-scores mayores de −2,5 tengan fracturas. De hecho, en la cohorte de estudio del National Osteoporosis Risk Assessment con más de 140.000 mujeres posmenopáusicas de Estados Unidos, casi un tercio de las mujeres que tenían fracturas también tenía puntuaciones de DMO en el rango «osteopénico». Por tanto, la toma de decisiones para el tratamiento no debe basarse únicamente en la DMO.
El tratamiento de la osteoporosis posmenopáusica se establece desde el punto de vista de la prevención primaria cuando se prescribe para aquellas mujeres con riesgo pero que no tienen una masa ósea baja ( T-score <− 2,5) o no tienen fracturas y desde el punto de vista del tratamiento para aquellas mujeres con enfermedad establecida, incluidas las fracturas osteoporóticas previas y/o una DMO muy disminuida. Por tanto, la selección de un régimen de tratamiento adecuado depende de si el tratamiento está diseñado principalmente para prevenir la pérdida de masa ósea o para reducir el riesgo de una probable fractura de columna o fractura no vertebral en sujetos de alto riesgo.
Medidas generales
Dieta
Calcio
Los suplementos de calcio deberían ser un complemento a los tratamientos farmacológicos en mujeres con osteoporosis establecida y deben formar parte de cualquier estrategia de prevención para mejorar la pérdida ósea independientemente de otras posibilidades de tratamiento. El incremento de la ingestión de calcio reduce el hiperparatiroidismo secundario observado con frecuencia en el envejecimiento y puede potenciar la mineralización de hueso de nueva formación. La evidencia de que el calcio y la vitamina D juntos, o de forma individual, reducen el riesgo de fractura en los sujetos osteoporóticos sigue siendo controvertida. Sin embargo, un reciente metaanálisis de ensayos clínicos intervencionistas con calcio y vitamina D mostró un aumento consistente aunque pequeño de la DMO y una reducción de las fracturas no vertebrales cuando se administraban al menos 1.200 mg de calcio combinado con más de 400 unidades de vitamina D. No se ha demostrado que los suplementos de calcio aislados reduzcan la incidencia de fracturas no vertebrales en mujeres de alto riesgo. Un ensayo clínico intervencionista de gran tamaño del WHI no mostró una reducción de las fracturas de cadera con suplementos diarios de 1.000 mg de calcio junto a 400 UI de vitamina D para todas las mujeres posmenopáusicas. Sin embargo, en las de más de 60 años, la reducción del riesgo fue estadísticamente significativa
. Resulta interesante destacar que los suplementos de calcio en esta cohorte se asociaron con un aumento del riesgo de cálculos renales del 17%. Esto se podría deber al hallazgo de que la ingesta basal de calcio en estas mujeres era en promedio de 1.100 mg/día. Las nuevas directrices del Institute of Medicine (IOM) recomiendan 1.200 mg al día de calcio en las mujeres de más de 70 años y 800 UI de vitamina D al día en el mismo grupo de edad. Ciertamente, con ingestas de más de 200 mg/día, aumenta el riesgo de nefrocalcinosis.
Vitamina D
La vitamina D es esencial para el mantenimiento del esqueleto y para potenciar la absorción de calcio. La insuficiencia de esta vitamina es un problema creciente; hasta dos tercios de todos los pacientes que tienen fractura de cadera se clasifican como deficientes en vitamina D ( cap. 252 ). No obstante, los resultados de diferentes ensayos clínicos aleatorizados son no concluyentes. Las personas ancianas que viven en centros de cuidados crónicos son especialmente vulnerables al déficit de vitamina D y se pueden beneficiar de los suplementos. Un amplio ensayo de distribución aleatoria controlado con placebo (EDACP) demostró una reducción de un 33% en las fracturas de cadera en personas institucionalizadas tratadas con calcio y vitamina D en comparación con aquellas que recibían placebo
. En otro ensayo clínico, la administración intermitente de vitamina D a dosis altas redujo las fracturas no vertebrales alrededor de un tercio entre personas ancianas ambulatorias . En varones y mujeres ancianos de Nueva Inglaterra, la combinación de citrato de calcio y 700 UI de vitamina D disminuyó el riesgo de fracturas no vertebrales en un tercio . Sin embargo, en un reciente y amplio estudio poblacional con calcio y vitamina D, el suplemento de éstos no tuvo efecto sobre las fracturas no vertebrales, aunque el cumplimiento y las concentraciones de vitamina D no estaban suficientemente bien documentados para excluir el efecto de forma concluyente. Varios metaanálisis recientes sugieren que para tener eficacia sobre las fracturas son precisas 800 UI/día de vitamina D. Aparte de los potenciales efectos positivos de los suplementos con vitamina D sobre el hueso, sobre todo en mujeres ancianas, la vitamina D también puede potenciar la fuerza muscular y se ha demostrado que disminuye el riesgo de caídas. Para la mayoría de los individuos con osteoporosis, es suficiente una dosis de vitamina D de 800 UI/día para mantener concentraciones adecuadas de 25-hidroxivitamina D. Sin embargo, en aquellos pacientes con masa muscular baja y concentraciones insuficientes o deficientes de 25-hidroxivitamina D (es decir, <20 ng/ml), es seguro y eficaz administrar 50.000 UI de ergocalciferol (vitamina D 2 ) o colecalciferol (vitamina D 3 ) una vez a la semana para restablecer las concentraciones de vitamina D al rango normal. Actualmente se están revisando los límites superiores de los suplementos de vitamina D para determinar si existe toxicidad con las dosis más altas.
Se han empleado análogos de vitamina D en el tratamiento de la osteoporosis desde el inicio de la década de 1980. Sin embargo, esta área sigue siendo controvertida. Las dosis altas de 1,25-dihidroxivitamina D aumentan la masa ósea, pero la mayoría de los pacientes desarrolla hipercalciuria y/o hipercalcemia. A dosis de 0,5 μg/día, disminuye la tasa de fracturas vertebrales y no vertebrales e incrementa la densidad ósea, según se observó en un ensayo clínico pequeño. Otros estudios han encontrado poco beneficio con una ventana terapéutica estrecha, sobre todo en relación con la función renal y la hipercalcemia. Actualmente, no se recomiendan los análogos de la vitamina D para el tratamiento de la osteoporosis. Un subgrupo de pacientes con insuficiencia renal (enfermedad renal crónica >3) y niveles elevados de PTH pueden beneficiarse de suplementos con calcitriol.
Actividad física
El reposo en cama o la inmovilidad, sobre todo en personas ancianas, puede provocar una pérdida rápida de hueso. Además, el número de caídas aumenta con la edad y el número de caídas que desencadenan fracturas también aumenta. Un metaanálisis realizado por el Cochrane Review Group demostró que la fuerza muscular, el reentrenamiento del equilibrio, la evaluación de los riesgos en el hogar, la interrupción de los medicamentos psicotrópicos y el empleo de programas multidisciplinarios de valoración de factores de riesgo son beneficiosos en la protección contra las caídas. Un enfoque alternativo es reducir las cargas aplicadas en la cadera durante la caída utilizando materiales acolchados. Los protectores de cadera han demostrado disminuir el riesgo de fracturas de cadera al menos en una población, aunque el cumplimiento suele ser pobre. Un estudio más reciente no pudo demostrar la eficacia de estos dispositivos en mujeres ancianas ingresadas en un geriátrico. La actividad física regular, incluidos los ejercicios aeróbicos, de carga de peso y los ejercicios de resistencia, es eficaz para aumentar la DMO de la columna y la resistencia muscular en mujeres posmenopáusicas, pero no se han realizado estudios a gran escala que establezcan si estas intervenciones disminuyen el riesgo de fractura.
Estilo de vida
Otras intervenciones, incluido dejar de fumar y disminuir la ingestión de alcohol, deben tenerse en cuenta dentro de la estrategia de medicina preventiva del sujeto. Sin embargo, hasta la fecha, los estudios no son concluyentes en lo referente a cómo estos cambios en el estilo de vida afectan al riesgo global de fractura.
Tratamiento médico
Existe amplia evidencia que indica que un programa de intervención intensivo puede tener éxito en disminuir el riesgo de fractura y mejorar la calidad de vida en mujeres posmenopáusicas con osteoporosis preexistente. Se dispone de diversas opciones farmacológicas, y éstas pueden ser clasificadas según su mecanismo de acción. Los dos grupos principales de fármacos para la osteoporosis son 1) antirresorptivos (es decir, agentes que bloquean la resorción inhibiendo los osteoclastos) y 2) anabólicos (es decir, fármacos que estimulan la formación de hueso actuando principalmente sobre los osteoblastos).
Fármacos antirresortivos
Los fármacos antirresortivos inhiben la resorción ósea suprimiendo la actividad de los osteoclastos. Al retrasar el ciclo de reestructuración, se permite la formación de hueso para alcanzar la resorción, potenciando así la mineralización de la matriz y estabilizando la microarquitectura trabecular. Los fármacos antirresortivos aumentan la DMO y disminuyen el riesgo de fractura, pero su eficacia es variable.
Estrógenos
La terapia sustitutiva con estrógenos durante mucho tiempo se consideró la piedra angular del tratamiento de las mujeres posmenopáusicas con osteoporosis. Funciona disminuyendo la resorción ósea a través de la inhibición del envío de señales de citocinas desde el osteoblasto hasta el osteoclasto, incrementando así la DMO. La sustitución con estrógenos inhibe la pérdida ósea cortical y trabecular y la DMO generalmente aumenta del 3% al 5% después de 3 años
. No parece existir un efecto adictivo con la progesterona sobre la masa ósea en mujeres que también son tratadas con estrógenos. A la inversa, la progesterona es una parte importante de la terapia sustitutiva con hormonas en mujeres con útero, dado que previene el desarrollo de hiperplasia endometrial y de carcinoma. En el WHI, los estrógenos y la progesterona disminuyeron el riesgo de fractura de cadera en un tercio
. Las dosis bajas conjugadas de estrógenos (0,3 o 0,45 mg/día) y las dosis ultrabajas de estradiol aumentan la DMO y han sido aprobadas para la prevención de la pérdida ósea, aunque no se ha establecido la eficacia antifractura de estos preparados. El cese de los estrógenos produce una pérdida ósea mensurable (del 3% al 5% en el primer año), aunque no está claro si esto se traduce en un incremento del riesgo de fractura.
Existe bastante preocupación sobre los riesgos no esqueléticos asociados con el tratamiento a largo plazo con estrógenos y estrógenos en combinación con progesterona ( cap. 248 ). Particularmente preocupante es el aumento del riesgo de cáncer de mama asociado al uso a largo plazo de estrógenos y progesterona. En el WHI, se observó un incremento del 26% del riesgo de cáncer de mama invasivo en un período de seguimiento de 5,2 años
. Por tanto, el tratamiento sustitutivo con estrógenos está contraindicado en cualquier mujer con antecedentes de cáncer de mama; se recomienda realizar mamografías anuales en todas las mujeres en tratamiento con terapia hormonal sustitutiva. Los estudios previos casos y control retrospectivos sugieren que los estrógenos podrían reducir la enfermedad arterial coronaria; sin embargo, en el WHI, el riesgo de infarto de miocardio o de muerte por enfermedad coronaria fue un 29% más alto en mujeres que recibían la terapia combinada . La enfermedad tromboembólica también aumenta más de tres veces con la terapia hormonal sustitutiva
. Por tanto, el empleo de estrógenos y/o estrógenos en combinación con progestágenos para la prevención y/o tratamiento de la osteoporosis ha caído de forma drástica. Además, la disponibilidad de nuevos fármacos antirresortivos más eficaces para el tratamiento de la osteoporosis ha disminuido el entusiasmo de la terapia hormonal primaria en la mujer osteoporótica.
Moduladores selectivos del receptor de estrógenos
Los moduladores selectivos del receptor de estrógeno, como el tamoxifeno y el raloxifeno, también inhiben la resorción ósea bloqueando la liberación de citocinas por los osteoblastos. Ambos han demostrado disminuir la pérdida ósea en mujeres posmenopáusicas con cáncer de mama, pero únicamente el raloxifeno está aprobado por la Food and Drug Administration (FDA) de EE.UU. para la prevención y el tratamiento de la osteoporosis.
Ambos fármacos bloquean las acciones de los estrógenos sobre la mama pero actúan como agonistas estrogénicos sobre el hueso; el tamoxifeno, pero no el raloxifeno, tiene propiedades agonistas estrogénicas sobre el útero y se asocia con un mayor riesgo de carcinoma endometrial con el empleo a largo plazo. Ambos agentes han sido asociados con una reducción de los nuevos casos de cáncer de mama cuando se administran como profilaxis en pacientes de alto riesgo
. Las concentraciones de colesterol asociado a lipoproteínas de baja densidad también disminuyen en pacientes tratados con estos moduladores selectivos del receptor de estrógenos. El raloxifeno aumenta levemente la DMO de la columna (como lo hace el tamoxifeno) y disminuye el riesgo de fracturas vertebrales en un 40%, aunque no tiene efectos sobre las fracturas no vertebrales
. Con la terapia con raloxifeno pueden ocurrir sofocos, calambres musculares en las piernas y mayor riesgo de desarrollar trombosis venosa profunda. La dosis recomendada de raloxifeno es de 60 mg una vez al día.
La selectividad tisular de estos moduladores selectivos del receptor de estrógeno y de otros fármacos que están siendo investigados es un tema de gran interés científico. El raloxifeno y el estrógeno se unen a la misma región del receptor estrogénico, pero inducen cambios conformacionales diferentes en el receptor. Se reclutan proteínas coactivadoras y cosupresoras al complejo ligando receptor, y se cree que estos factores de transcripción finalmente determinan la actividad del complejo nuclear. Dado que el reclutamiento también depende de la localización, es muy probable que exista una selectividad tisular importante para estas dos sustancias. Se están investigando nuevos agentes para facilitar complejos concretos y reagrupaciones dentro del núcleo; éstos se encuentran actualmente en fase de estudios preclínicos y clínicos.
Bifosfonatos
Los bifosfonatos son los fármacos antirresortivos más ampliamente prescritos y con frecuencia se consideran el tratamiento de primera línea en la osteoporosis posmenopáusica grave. Estos fármacos son análogos del pirofosfato con sustitución de carbono que se unen de forma estrecha a los cristales de hidroxiapatita. Se piensa que estos agentes suprimen directamente la resorción inhibiendo la unión de los osteoclastos y potenciando la muerte celular programada. La primera generación de bifosfonatos incluía etidronato y clodronato. Ninguno está aprobado para el tratamiento de la osteoporosis aunque el etidronato se emplea ampliamente «fuera de indicaciones» y en Europa. La dosis de etidronato es de 400 mg/día durante 2 semanas cada 3 meses. El fármaco tiene efectos secundarios gastrointestinales y la disminución del riesgo de fracturas vertebrales es importante con este fármaco. Los bifosfonatos de segunda generación que contienen nitrógeno, el alendronato y risedronato, son eficaces en la supresión de la resorción ósea e incrementan la DMO. En mujeres posmenopáusicas con osteoporosis definida, el alendronato y el risedronato disminuyeron las fracturas vertebrales, de cadera y no vertebrales alrededor del 50%, sobre todo durante el primer año de tratamiento
. Al igual que otros fármacos antirresortivos, el incremento de la DMO con alendronato y el risedronato es responsable de una pequeña proporción de su eficacia antifractura. Por tanto, el seguimiento con medidas de DXA puede subestimar de forma importante la reducción del riesgo de fractura. Los ensayos clínicos recientes han demostrado que estos fármacos pueden ser administrados de forma segura durante al menos 7 años sin afectar de forma importante la resistencia ósea. Además, el cese de la administración de alendronato después de 5 años provoca una mínima pérdida de hueso en los 5 años siguientes. Ambos fármacos tienen un perfil de seguridad excelente, aunque se han descrito esofagitis erosivas como complicación grave de todos los bifosfonatos que contienen nitrógeno. Se ha demostrado que la administración una vez a la semana de alendronato disminuye la prevalencia de esofagitis inducida por el fármaco y actualmente ambos bifosfonatos están indicados para tratamientos una vez a la semana. Recientemente, la FDA ha autorizado el uso de risedronato en dosis una vez al mes (150 mg/mes) para el tratamiento de la osteoporosis.
La FDA de EE.UU. ha autorizado dos nuevos bifosfonatos, que han llegado al mercado en los últimos 5 años: ibandronato y zoledronato. El ibandronato se administra en una dosis mensual única de 150 mg o por vía intravenosa (3 mg) cada 3 meses. Suprime la reabsorción ósea y reduce la tasa de fracturas vertebrales, aunque su eficacia en fracturas no vertebrales es algo menor que la de alendronato o residronato
. El cumplimiento con el régimen una vez al mes es mayor que con el régimen de dosificación semanal, aunque los datos a largo plazo no son alentadores. El zoledronato también está aprobado para la prevención y el tratamiento de la osteoporosis
. Se administra como una infusión intravenosa única durante 15 minutos (5 mg) una vez al año. En amplios estudios controlados aleatorizados se ha establecido de forma inequívoca su eficacia antifractura en las fracturas de cadera, vertebrales y otras no vertebrales. Recientemente, la FDA ha autorizado el uso de zoledronato para la prevención de la osteoporosis mediante la administración del fármaco una vez cada 2 años. Ambos nuevos bifosfonatos pueden producir efectos adversos de primera dosis, tales como dolor articular, rigidez y febrícula. No persisten con la administración repetida. Sin embargo, la FDA advierte que la administración de ácido zoledrónico debería realizarse durante 1 hora y no en 15 minutos para disminuir cualquier riesgo, aunque pequeño, de daño renal. El ácido zoledrónico intravenoso está autorizado también para el tratamiento de la hipercalcemia de las neoplasias malignas ( cap. 186 ) y del mieloma múltiple y como tratamiento paliativo de la enfermedad metastásica.
Se dispone de otros bifosfonatos para su uso no autorizado que están siendo estudiados para el tratamiento de la osteoporosis. El pamidronato intravenoso también está disponible desde mitad de los años 90 para el tratamiento de la enfermedad de Paget ( cap. 255 ) y de la hipercalcemia maligna ( cap. 186 ). En la actualidad se utiliza también para el tratamiento de mujeres osteoporóticas que no pueden tolerar los bifosfonatos orales, aunque no ha sido autorizado formalmente por la FDA para esta indicación, ni tampoco se ha demostrado su eficacia antifractura. Las dosis se encuentran entre 30 y 90 mg administrados cada 3-9 meses. Con este fármaco se pueden producir reacciones de hipersensibilidad de tipo agudo y retardada, y su uso está contraindicado en pacientes con déficit de vitamina D ya que puede disminuir de forma rápida el calcio sérico.
En relación con los bifosfonatos, se han comunicado dos efectos adversos poco frecuentes. La osteonecrosis de la mandíbula es una afección devastadora que se asocia con destrucción de la mandíbula tras una intervención dental ( cap. 256 ). Se ha observado en pacientes que toman bifosfonatos, particularmente los que reciben tratamiento intravenoso y que también presentan enfermedades asociadas como mieloma múltiple o cáncer de mama metastásico. Su prevalencia verdadera es desconocida pero es probable que sea de aproximadamente 1 cada 250.000 casos y es poco frecuente en mujeres y varones tratados por osteoporosis y sanos por lo demás. No obstante se debe tener precaución a la hora de recomendar cirugía dental a pacientes que toman un bifosfonato. Las fracturas subtrocantéricas son otra afección que se puede asociar con el uso a largo plazo de bifosfonatos. Estas fracturas mediodiafisarias se suelen producir en mujeres de mediana edad que toman un bifosfonato oral durante varios años, asociado con frecuencia a tratamiento con glucocorticoides o al uso de un fármaco antirresortivo adicional. El paciente suele aquejar dolor en la pierna antes de la fractura, y en las radiografías se observa un engrosamiento cortical antes de la fractura. La prevalencia verdadera es desconocida, pero probablemente es extremadamente rara y se cree que la etiología está relacionada con un exceso de supresión del recambio óseo. El tratamiento no es diferente de cualquier tratamiento quirúrgico, aunque se recomienda la suspensión del bifosfonato.
Calcitonina
La calcitonina es un péptido de 32 aminoácidos producido normalmente por las células C tiroideas. Los osteoclastos tienen receptores de calcitonina y ésta inhibe de forma rápida la resorción ósea. La calcitonina de salmón es más potente que la humana y es el tratamiento de elección. Están aprobadas para el tratamiento de la osteoporosis posmenopáusica la calcitonina nasal y subcutánea. Sin embargo, carecemos de evidencias que favorezcan un efecto importante de esta hormona sobre la pérdida ósea o la eficacia frente a fracturas. En un EDACP en mujeres con osteoporosis posmenopáusica, la administración de calcitonina nasal, 200 UI/día, redujo la incidencia de fracturas vertebrales en un tercio
. Sin embargo, los defectos metodológicos en este ensayo han disminuido el entusiasmo por este agente como tratamiento de primera línea para la osteoporosis. En al menos un estudio controlado con placebo, la calcitonina nasal disminuyó el dolor asociado con las fracturas vertebrales nuevas. La dosis recomendada de calcitonina nasal es de 200 UI/día, y la de la calcitonina subcutánea es de 100 UI/día. Los efectos secundarios son infrecuentes con la calcitonina nasal e incluyen congestión nasal y rubeosis. Con la administración subcutánea no son infrecuentes las náuseas.
Ranelato de estroncio
El ranelato de estroncio se administra por vía oral y estimula la captación de calcio por el hueso al mismo tiempo que inhibe la resorción ósea. Se cree que tiene cierta actividad anabólica, aunque el mecanismo concreto de acción sobre el hueso una vez incorporado es desconocido. En un EDACP en mujeres posmenopáusicas con enfermedad establecida, el estroncio diario redujo el riesgo de fracturas vertebrales en un 40%
. Sin embargo, se observó un efecto limitado, estadísticamente significativo, sobre las fracturas no vertebrales en una pequeña subpoblación de mujeres en un análisis retrospectivo. Este fármaco está aprobado por las agencias reguladoras europeas pero no por la FDA de EE.UU.
Agentes anabólicos
En el año 2002 se introdujo una nueva familia de fármacos antiosteoporosis. Éstos son los denominados anabólicos, agentes que estimulan la formación de hueso más que la resorción del mismo. Por tanto, estos agentes potencian la reestructuración ósea y difieren bastante de los fármacos antirresortivos, que disminuyen el recambio óseo. La PTH 1-34 (teriparatida) fue el primero de ese grupo de fármacos aprobado por la FDA.
El fármaco anabólico prototípico fue el fluoruro sódico, que fue muy empleado en los años 70 y 80 por su capacidad de estimular la nueva formación de hueso. Sin embargo, un EDACP realizado en 1990 estableció que aunque se producía un incremento importante en la DMO, el riesgo de fracturas no vertebrales se incrementaba. Contrariamente al fluoruro sódico, la PTH sintética (PTH 1-34 ) fue aprobada por la FDA estadounidense para el tratamiento de la osteoporosis posmenopáusica porque no sólo aumenta la masa ósea sino que también reduce las fracturas. En el EDACP más amplio realizado utilizando teriparatida en mujeres posmenopáusicas con osteoporosis grave, la dosis de PTH de 20 μg/día, administrada por vía subcutánea, redujo las fracturas de columna y las fracturas no vertebrales más de un 50%, y al mismo tiempo aumentó de forma sustancial la DMO lumbar (es decir, 8%/año)
. Se encontraron hallazgos similares en varones con osteoporosis tratados durante 11 meses. Desgraciadamente, el ensayo con PTH en mujeres posmenopáusicas se interrumpió después de 20 meses por preocupación relacionada con el desarrollo de osteosarcoma en ratas tratadas con dosis altas de PTH 1-34 . Sin embargo, los estudios retrospectivos han encontrado que no existe asociación entre el osteosarcoma y el hiperparatiroidismo primario o secundario, y sólo se han notificado dos casos de osteosarcoma en pacientes tratados con PTH. Más recientemente, la PTH recombinante humana (PTH 1-84 ) ha demostrado beneficios similares
. Actualmente, se recomienda que el tratamiento con PTH se limite a aquellos individuos con osteoporosis de moderada a grave y sólo durante 2 años.
A pesar del atractivo de utilizar fármacos anabólicos con antirresortivos, ninguna evidencia indica que la combinación de estos fármacos sea aditiva o sinérgica. Contrariamente a lo que ocurre con los bifosfonatos, la interrupción de la PTH puede provocar una pérdida ósea del 3% al 4% durante el primer año después de su interrupción. Este efecto postratamiento se previene añadiendo un fármaco antirresortivo cuando se interrumpe la PTH. En general, la PTH se tolera bien, aunque pueden producirse náuseas, rubeosis, hipotensión e hipercalcemia leve asintomática (es decir, calcio sérico <11,0 mg/dl). Los factores limitantes principales han sido el coste y el cumplimiento.
Vertebroplastia/Cifoplastia
La vertebroplastia (inyección percutánea de cemento en una vértebra colapsada para estabilizarla) y la cifoplastia (el uso de un balón para distender/insuflar el cuerpo vertebral antes de la inyección del cemento en un intento de restaurar la altura y el ángulo del cuerpo vertebral) se utilizan ampliamente para tratar el dolor de las fracturas por compresión vertebral. A pesar de los prometedores resultados del alivio del dolor en comparación con el tratamiento estándar, no se han observado beneficios en comparación con el procedimiento simulado
.
Tratamiento
- Últimos artículos sobre Evaluación diagnóstica
- Resultados sobre osteoporosis & Evaluación diagnóstica
Osteoporosis en varones
Epidemiología
La osteoporosis en varones está siendo diagnosticada cada vez con mayor frecuencia. Esto puede ser debido a una mayor preocupación con respecto a la presentación clínica, el papel del cribado de la densidad ósea y la mayor comprensión de la patogenia de la osteoporosis, sobre todo en hombres mayores. El 30% de todas las fracturas de cadera y vertebrales se producen en hombres, y uno de cada seis hombres padecerá una fractura de cadera en la etapa tardía de la vida.
Manifestaciones clínicas
La presentación clínica con frecuencia es diferente de la de las mujeres, especialmente en relación con el momento del diagnóstico después del inicio de los síntomas. La queja más frecuente es dolor de espalda si hay compresión vertebral. Las medidas de densidad ósea se realizan con mucha menos frecuencia en varones, y suelen realizarse después de que aparezcan los síntomas, una situación muy diferente de lo que ocurre en mujeres posmenopáusicas.
Fisiopatología
Las causas secundarias de osteoporosis dominan esta enfermedad en el caso de los hombres. Los factores etiológicos principales de la osteoporosis en los varones son el hipogonadismo y la hipercortisolemia, y deben ser descartados independientemente de la presentación fenotípica. Sin embargo, algunas otras enfermedades, incluida la enteropatía por gluten, la resección o la derivación gástricas, y el abuso de alcohol son más frecuentes en varones que en mujeres con osteoporosis. La hipercalciuria (con o sin cálculos renales) que se asocia con el hiperparatiroidismo secundario casi siempre se produce en varones y es una causa frecuente de pérdida de masa ósea en varones jóvenes. Por el contrario, la anorexia es extremadamente infrecuente en varones y la tríada del atleta, muy característica de las mujeres corredoras (es decir, ejercicio, hipogonadismo y baja masa ósea), es infrecuente, aunque no insólita, en varones.
La falta de andrógenos da lugar a un déficit esquelético. El pico de masa ósea está claramente disminuido en los pacientes varones jóvenes con insuficiencia de andrógenos, independientemente de si esto es debido a un hipogonadismo hipogonadotrópico idiopático, a un síndrome de Klinefelter o a un retraso constitucional de la pubertad. El empleo de análogos de hormona liberadora de gonadotropina de larga acción que bloquean la producción de andrógenos y que se administran en el tratamiento del cáncer de próstata, también se asocia con una pérdida importante de masa ósea en la etapa tardía de la vida. Los hombres con insuficiencia gonadal primaria, hemocromatosis, hipogonadismo hiperprolactinémico y otras enfermedades del hipotálamo o de la hipófisis, con frecuencia tienen una masa ósea muy baja. Los andrógenos actúan estimulando directamente la formación de hueso dado que los osteoblastos tienen receptores de andrógenos. Sin embargo, la testosterona probablemente bloquee también la resorción ósea y pueda alterar la liberación de TNF, IL-6 e IL-1. No es sorprendente que los estrógenos también desempeñen un papel importante en el esqueleto masculino. La inhibición de la aromatización de la testosterona (es decir, de la aromatasa P-450) hacia estrógenos, ya sea por una mutación genética o por fármacos, produce una pérdida ósea significativa.
Las terapias para la osteoporosis en varones se centran en la identificación de la causa subyacente y el tratamiento farmacológico que también se emplea en mujeres. El hipogonadismo puede tratarse de forma eficaz con sustitución con andrógenos, aunque se debe tener precaución en varones ancianos por el riesgo de cáncer de próstata. La hipercalciuria puede disminuirse utilizando hidroclorotiazida, que también puede potenciar la densidad ósea en varones. Se ha demostrado que el alendronato previene la pérdida ósea y reduce las fracturas en varones con osteoporosis idiopática o con osteoporosis secundaria a situaciones de déficit de andrógenos
. La PTH 1-34 también ha sido aprobada para el tratamiento de la osteoporosis en varones, dado que también puede potenciar la densidad ósea y evitar fracturas. En un ensayo clínico de gran tamaño en varones con cáncer de próstata limitado que tomaban agonistas liberadores de gonadotropinas, el denosumab redujo las fracturas y evitó la pérdida ósea. Este fármaco, cuando sea autorizado por la FDA, puede ser el tratamiento más apropiado para la cada vez mayor cohorte de varones que reciben terapia antineoplásica agresiva. Los moduladores selectivos del receptor de andrógenos están actualmente en desarrollo y pueden aportar un nuevo enfoque para el tratamiento de la osteoporosis en varones.
Tratamiento
- Últimos artículos sobre Osteoporosis en varones
- Resultados sobre osteoporosis & Osteoporosis en varones
Lecturas Recomendadas
Cummings S.R., Ensrud K., Delmas P.D., et. al.: Lasofoxifene in postmenopausal women with osteoporosis. N Engl J Med 2010; 362: pp. 686-696. En un ensayo clínico aleatorizado de mujeres posmenopáusicas con osteoporosis, el lasofoxifeno (0,5 mg/día) produjo una disminución del riesgo de fracturas, cáncer de mama, accidentes cerebrovasculares y enfermedad coronaria aunque también produjo un aumento de accidentes tromboembólicos venosos.
Donaldson M.G., Cawthon P.M., Lui L.Y., et. al.: Estimates of the proportion of older white men who would be recommended for the pharmacologic treatment by the new U.S. National Osteoporosis Foundation guidelines. J Bone Miner Res 2010; 25: pp. 1506-1511. Se estima que aproximadamente el 35% de los varones blancos de EE.UU. de edad igual o superior a los 65 años y el 50% de los de edad igual o superior a los 75 años serán recomendados para el tratamiento farmacológico.
Favus M.J.: Bisphosphonates for osteoporosis. N Engl J Med 2010; 363: pp. 2027-2035. Revisión.
Grossman J.M., Gordon R., Ranganath V.K., et. al.: American College of Rheumatology 2010 recommendations for the prevention and treatment of glucocorticoid-induced osteoporosis. Arthritis Care Res (Hoboken) 2010; 62: pp. 1515-1526. Guías clínicas de consenso.
Papaioannou A., Morin S., Cheung A.M., et. al.: 2010 clinical practice guidelines for the diagnosis and management of osteoporosis in Canada: summary. CMAJ 2010; 182: pp. 1864-1873. Guías clínicas de consenso.
Rachner T.D., Khosla S., Hofbauer L.C.: Osteoporosis: now and the future. Lancet 2011; 377: pp. 1276-1287. Revisión.
Sanders K.M., Stuart A.L., Williamson E.J., et. al.: Annual high-dose oral vitamin D and falls and fractures in older women: a randomized controlled trial. JAMA 2010; 303: pp. 1815-1822. En un ensayo clínico controlado, las dosis altas de vitamina D aumentaban sorprendentemente el riesgo de caídas y fracturas.
U.S. Preventive Services Task Force, Force : Screening for osteoporosis: U.S. Preventive Services Task Force recommendation statement. Ann Intern Med 2011; 154: pp. 356-364. Las guías clínicas recomiendan el cribado en mujeres pero no claramente en varones.
Watts N.B., Bilezikian J.P., Camacho P.M., et. al.: American Association of Clinical Endocrinologists Medical Guidelines for Clinical Practice for the diagnosis and treatment of postmenopausal osteoporosis. Endocr Pract 2010; 16: pp. 1-37. Guías clínicas de consenso.
Bolignano, Davide, Mattace-Raso, Francesco, Sijbrands, Eric J.G., Zoccali, Carmine. Ageing Research Reviews, 2014-2-1, Volume 14, Elsevier B.V..
Pieper, Marjoleine J.C., van Dalen-Kok, Annelore H., Francke, Anneke L., van der Steen, Jenny T., Scherder, Erik J.A., Husebø, Bettina S., Achterberg, Wilco P.. Ageing Research Reviews, 2013-8-1, Volume 12, Issue 4, Elsevier B.V..
Duggan, Sinead N., Smyth, Niamh D., Murphy, Anne, MacNaughton, David, O’Keefe, Stephen J.D., Conlon, Kevin C.. Clinical Gastroenterology and Hepatology, 2014-1-1, Volume 12, Issue 2, AGA Institute.
SEEN -April 30, 2015
SIR -February 1, 2014
AGA Institute -April 30, 2015
 Vademécum
Vademécum
Leave a Comment