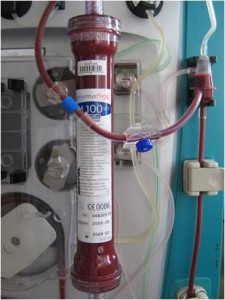
 La Fracción de filtración (FF) es la cantidad de agua plasmática que retiramos respecto de la que introducimos en el filtro.
La Fracción de filtración (FF) es la cantidad de agua plasmática que retiramos respecto de la que introducimos en el filtro.
La FF recomendada para los tratamientos de depuración extracorpórea es del 25% o inferior. Si utilizamos alto volumen puede aceptarse hasta 30%.
Una FF adecuada, junto a la anticoagulación pautada contribuye a la prolongación del tiempo de utilidad y efectividad del filtro.
FF= Quf/Qpl x 100
Quf= Flujo de ultrafiltrado
Qpl= Flujo plasmático
Quf= Efluente (ml/h) – Diálisis (ml/h)
Qpl= Qs x (1-Hto) + Reposición (solo la parte pre filtro)
Qs= Flujo de sangre (multiplicar x 60 para llevar a ml/h)
Ejemplo: Paciente de 70 kg al que se le programa HDFVVC. Reposición post filtro: 2000 ml/h, Diálisis: 1000 ml/h, Efluente: 3000 ml/h Hematocrito: 0.28, Flujo de sangre: 250 ml/min. Dosis de HDFVVC: 43 ml/kg/h (alto volumen ≥ 35 ml/kg/h)
FF= (3000-1000 )/((250 x 60)x (1-0.28) ) x 100
FF= (2000 )/((15000)x (0.72) ) x 100
FF= (2000 )/10800 x 100
FF= 0.185 x 100
FF= 18.5%
¿Como disminuir una FF > 25% y mantener igual dosis de HDFVVC?
Aumentar el flujo de sangre
Disminuir reposición y aumentar diálisis
Pasar la reposición a prefiltro
![]()
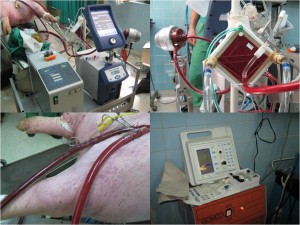

 El trabajo alerta sobre la necesidad de educación, vacunación, diagnóstico y tratamiento oportuno del virus de la influenza A (H1N1) en la población de pacientes trasplantados.
El trabajo alerta sobre la necesidad de educación, vacunación, diagnóstico y tratamiento oportuno del virus de la influenza A (H1N1) en la población de pacientes trasplantados.
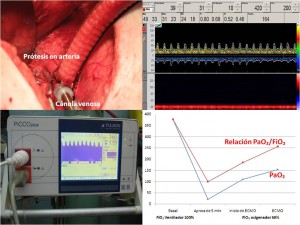 Se realizó ECMO veno – arterial, con canulación de vena y arteria femoral izquierda. Se monitorizó a través de catéter de PiCCO (monitorización hemodinámica por análisis de la curva de contorno del pulso y termodilución transpulmonar) en arteria femoral derecha. Se realizo monitorización de la hemodinámia cerebral y detección de microémbolos a través de sonografía doppler transcraneal. La canulación arterial se realizó previo implante de una prótesis de dacrón revestido de colágeno, que posteriormente hubo que retirar y recanular por sangrado a través de la prótesis. En este caso pudimos utilizar una mezcla exacta de aire comprimido y oxigeno, de acuerdo a necesidades. Después de una muestra basal de gases arteriales, se retiró la ventilación mecánica (sedado y relajado), provocando acidosis respiratoria e hipoxemia que fue resuelta tras la instauración del ECMO.
Se realizó ECMO veno – arterial, con canulación de vena y arteria femoral izquierda. Se monitorizó a través de catéter de PiCCO (monitorización hemodinámica por análisis de la curva de contorno del pulso y termodilución transpulmonar) en arteria femoral derecha. Se realizo monitorización de la hemodinámia cerebral y detección de microémbolos a través de sonografía doppler transcraneal. La canulación arterial se realizó previo implante de una prótesis de dacrón revestido de colágeno, que posteriormente hubo que retirar y recanular por sangrado a través de la prótesis. En este caso pudimos utilizar una mezcla exacta de aire comprimido y oxigeno, de acuerdo a necesidades. Después de una muestra basal de gases arteriales, se retiró la ventilación mecánica (sedado y relajado), provocando acidosis respiratoria e hipoxemia que fue resuelta tras la instauración del ECMO.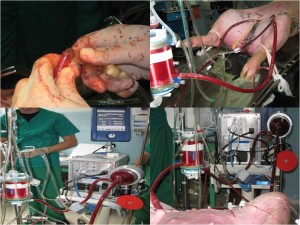 Hope, sirvió para demostrar que la practica y el entrenamiento se traduce en rapidez y éxito al enfrentar una nueva tecnología. Existen estrategias que ayudan a disminuir los efectos de la curva de aprendizaje, una de ellas es la experimentación animal. Se realizó ECMO veno – arterial, con canulación de vena femoral izquierda y arteria femoral izquierda. Se monitorizó a través de catéter en arteria femoral derecha, arteria axilar izquierda y catéter de Swan Ganz por vena yugular derecha. No existieron complicaciones técnicas a comentar. Durante seis horas de mantenimiento comprobamos la disminución de la albumina sérica, relacionada con los efectos de la respuesta inflamatoria.
Hope, sirvió para demostrar que la practica y el entrenamiento se traduce en rapidez y éxito al enfrentar una nueva tecnología. Existen estrategias que ayudan a disminuir los efectos de la curva de aprendizaje, una de ellas es la experimentación animal. Se realizó ECMO veno – arterial, con canulación de vena femoral izquierda y arteria femoral izquierda. Se monitorizó a través de catéter en arteria femoral derecha, arteria axilar izquierda y catéter de Swan Ganz por vena yugular derecha. No existieron complicaciones técnicas a comentar. Durante seis horas de mantenimiento comprobamos la disminución de la albumina sérica, relacionada con los efectos de la respuesta inflamatoria.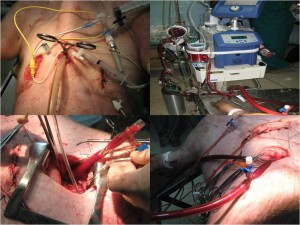 Walton, nuestro primer ECMO y además exitoso. Se realizó ECMO veno – arterial, con canulación de vena femoral izquierda y arteria femoral izquierda. Se monitorizó a través de catéter en arteria femoral derecha, arteria axilar derecha y catéter de Swan Ganz por vena yugular derecha. No existieron complicaciones a comentar. Después de cuatro horas de mantenimiento realizamos intervenciones que nos permitieron comprobar la diferencia de oxigenación entre sangre arterial femoral y arterial axilar en situación de falla respiratoria extrema, así como el mantenimiento de oxigenación y medio interno después de 30 minutos de parada cardio – respiratoria con mantenimiento de reflejos fotomotor y corneal.
Walton, nuestro primer ECMO y además exitoso. Se realizó ECMO veno – arterial, con canulación de vena femoral izquierda y arteria femoral izquierda. Se monitorizó a través de catéter en arteria femoral derecha, arteria axilar derecha y catéter de Swan Ganz por vena yugular derecha. No existieron complicaciones a comentar. Después de cuatro horas de mantenimiento realizamos intervenciones que nos permitieron comprobar la diferencia de oxigenación entre sangre arterial femoral y arterial axilar en situación de falla respiratoria extrema, así como el mantenimiento de oxigenación y medio interno después de 30 minutos de parada cardio – respiratoria con mantenimiento de reflejos fotomotor y corneal. La Fracción de filtración (FF) es la cantidad de agua plasmática que retiramos respecto de la que introducimos en el filtro.
La Fracción de filtración (FF) es la cantidad de agua plasmática que retiramos respecto de la que introducimos en el filtro.

Comentarios recientes